Estado de deficiência do sistema imunitário para responder aos agentes agressores. É definida como primária quando é dependente de fatores genéticos hereditários. A secundária/adquirida é causada por um fator externo.
É o ato de reduzir intencionalmente a atividade ou eficiência do sistema imunológico. É feita para diminuir rejeição em transplante de órgãos ou para tratamento de doenças autoimunes.
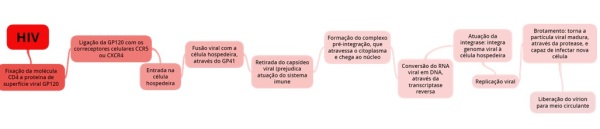
A SIDA só ocorre em um estágio tardio da infecção pelo vírus da imunodeficiência humana (HIV), um retrovírus que tem como alvo os linfócitos T com receptores CD4. O vírus está presente no sangue de pessoas infectadas, assim como em outros fluidos, como o sêmen, secreção vaginal e leite materno.
O HIV é um vírus e a SIDA é a condição que pode decorrer da infeção por esse vírus. Assim, pode ter-se uma infeção por HIV sem adquirir SIDA, sendo muitas as pessoas com infecção por HIV que vivem durante anos sem desenvolver SIDA.
- HIV:
- Epidemiologia
- De 1992 aos dias atuais, grande aumento de casos por exposição heterossexual, assumindo cada vez maior importância o número de casos em mulheres – feminização da epidemia.
- Atualmente a principal via de transmissão em crescimento é a heterossexual (58,3%).
- A região da África subsaariana é a mais atingida, 60% dos casos – mulheres representam 58% desse total.
- Entre 1980 e 2012 foram registrados 686.478 mil casos de AIDS no Brasil, dos quais 256.698 evoluíram para óbito por causa básica aids.
- Em São Paulo se concentra a maior parte da epidemia nacional – 33% dos casos do país.
- Estima-se em aproximadamente 132 mil o número de portadores de HIV com idade entre 15 e 49 anos no estado de SP.
- Entre 2003 e 2006, em torno de 42% dos portadores de HIV do estado de São Paulo chegavam aos serviços com a contagem de células de T-CD4 abaixo de 200, o que revela acesso tardio aos serviços de saúde. Essa taxa caiu para 30% em 2008 e 25% em 2012
- Até 2012, no estado de SP, dos 86,7% de casos notificados de que se tem informação sobre a provável forma de infecção, 74,8% são de transmissão heterossexual. O uso de drogas injetáveis responde por 11,3% restantes.
- Transmissão
- Sexual: A principal forma de exposição em todo o mundo é a sexual, sendo que a transmissão heterossexual, nas relações sem o uso de preservativo é considerada pela OMS como a mais frequente.
- Sanguínea: A transmissão sanguínea associada ao uso de drogas injetáveis é um meio muito eficaz de transmissão do HIV, devido ao uso compartilhado de seringas e agulhas. Essa via de transmissão adquire importância crescente em várias partes do mundo, como na Ásia, América Latina e no Caribe.
- Vertical: Decorrente da exposição da criança durante a gestação, parto ou aleitamento materno, vem aumentando devido à maior transmissão heterossexual. Na África, são encontradas as maiores taxas desta forma de infecção pelo HIV, da ordem de 30 a 40%; entretanto, em outras partes do mundo, como na América do Norte e Europa, situam-se em torno de 15 a 29%.
- Ocupacional: Ocorre quando profissionais da área da saúde sofrem ferimentos com instrumentos pérfuro-cortantes contaminados com sangue de pacientes portadores do HIV. Estima-se que o risco médio de contrair o HIV após uma exposição percutânea a sangue contaminado seja de aproximadamente 0,3%.
Fases clínicas
- Infecção aguda: Definida como as primeiras semanas da infecção pelo HIV, até o aparecimento dos anticorpos anti-HIV (soroconversão), que costuma ocorrer em torno da quarta semana após a infecção. Nessa fase, são produzidas diariamente bilhões de partículas virais e então, a viremia plasmática alcança níveis elevados e a pessoa se torna altamente infectante. A infecção pelo HIV é acompanhada por um conjunto de manifestações clínicas chamada Síndrome Retroviral Aguda (SRA), que se apresenta geralmente entre a primeira e a terceira semana após a infecção. Os principais achados clínicos de SRA incluem febre, adenopatia, faringite, exantema, mialgia e cefaleia. A SRA pode cursar com febre alta, sudorese e linfadenomegalia, comprometendo principalmente as cadeias cervicais anterior e posterior, submandibular, occipital e axilar. Podem ocorrer, ainda, esplenomegalia, letargia, astenia, anorexia e depressão. A sorologia para a infecção pelo HIV é geralmente negativa nessa fase, mas o diagnóstico pode ser realizado com a utilização de métodos moleculares para a detecção de RNA do HIV.
- Latência clínica ou fase assintomática: O estado clínico básico é mínimo ou inexistente. Alguns pacientes podem apresentar uma linfoadenopatia generalizada persistente, “flutuante” e indolor.
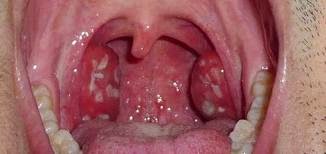
- Fase sintomática inicial: Nesta fase, o portador de HIV pode apresentar sinais e sintomas inespecíficos de intensidade variável, além de processos oportunistas de menor gravidade, principalmente na pele e nas mucosas. Pode apresentar sudorese noturna, fadiga, emagrecimento, diarreia, sinusopatias, candidíase oral e vaginal, gengivite, úlceras aftosas, herpes simples recorrente e herpes zoster.
- Síndrome da imunodeficiência adquirida: O aparecimento de infecções oportunistas e neoplasias é definidor da Síndrome da Imunodeficiência Adquirida (aids). Entre as infecções oportunistas destacam-se: pneumocistose, neurotoxoplasmose, tuberculose pulmonar atípica ou disseminada, meningite criptocócica e retinite por citomegalovírus. Além das infecções e das manifestações não infecciosas, o HIV pode causar doenças por dano direto a certos órgãos ou por processos inflamatórios, tais como miocardiopatia, nefropatia e neuropatias que podem estar presentes durante toda a evolução da infecção pelo HIV-1.
Diagnóstico
- Os testes para detecção da infecção pelo HIV podem ser divididos, basicamente, em quatro grupos: 1. Testes de detecção de anticorpos; 2. Testes de detecção de antígenos; 3. Testes de amplificação do genoma do vírus; e 4. Técnicas de cultura viral.
- ELISA – ensaio imunoenzimático: muito utilizado na triagem de anticorpos contra o vírus
- Imunofluorescência indireta: usado na etapa de confirmação sorológica
- Western-blot: padrão ouro para confirmar o resultado reagente na etapa de triagem. Alta especificidade e sensibilidade, porém, com elevado custo
- Radioimunoprecipitação: detecção dos anticorpos decorre de reações com antígenos radioativos
Contagem de células CD4+ em sangue periférico
- Maior que 500 células/mm3: Estágio da infecção pelo HIV com baixo risco de doença. Há boa resposta às imunizações de rotina e boa confiabilidade nos testes cutâneos de hipersensibilidade tardia, como o PPD.
- Entre 200 e 500 células/mm3: Estágio caracterizado por surgimento de sinais e sintomas menores ou alterações constitucionais. Risco moderado de desenvolvimento de doenças oportunistas. Nesta fase, podem aparecer candidíase oral, herpes simples recorrente, herpes zoster, tuberculose, leucoplasia pilosa, pneumonia bacteriana.
- Entre 50 e 200 células/mm3: Estágio com alta probabilidade de surgimento de doenças oportunistas como pneumocistose, toxoplasmose de SNC, neurocriptococose, histoplasmose, citomegalovirose localizada.
- Menor que 50 células/mm3: Estágio com grave comprometimento de resposta imunitária. Alto risco de surgimento de doenças oportunistas como citomegalovirose disseminada, sarcoma de Kaposi, linfoma não-Hodgkin e infecção por micobactérias atípicas. Alto risco de vida com baixa sobrevida.




Comentários